
Hämatopoetische Stammzellen – die Alleskönner aus dem Nabelschnurblut
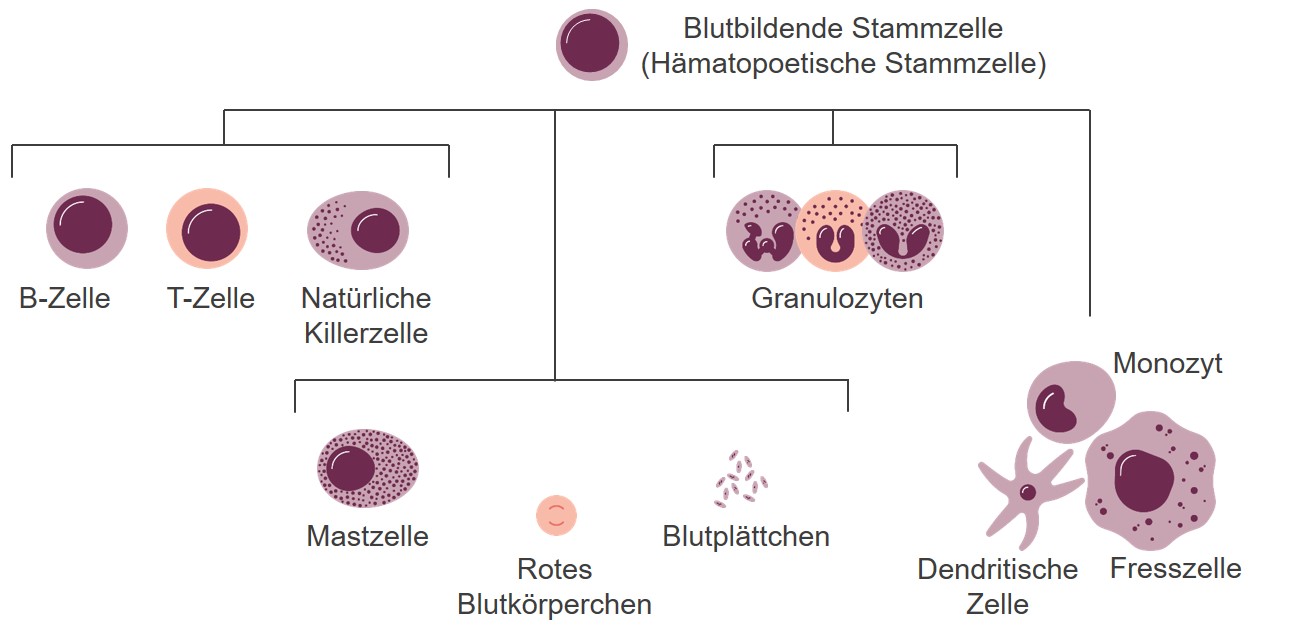
Nabelschnurblut (NSB) enthält besonders viele hämatopoetische Stammzellen (HSC). Diese sind der Ursprung aller Blutzellen (vgl. Abb. 1), die im menschlichen Körper lebenslang neu gebildet werden müssen. HSC sind daher lebenswichtig für die Aufrechterhaltung der Funktion des Blutes, insbesondere für den Sauerstofftransport und die Immunabwehr. Darüber hinaus sind im NSB auch mesenchymale Stammzellen und endotheliale Stammzellen sowie Zellen des angeborenen und erworbenen Immunsystems enthalten. [1]
Eine Besonderheit aller Zellen im NSBist, dass sie besonders jung und teilungsfähig sind und darüber hinaus nicht belastet oder beschädigt durch Infektionen, Krankheiten oder Mutationen sind. [2]
Vita 34, FamiCord AG
Wie kommen so viele hämatopoetische Stammzellen in das Nabelschnurblut?
Im Knochenmark des Menschen werden lebenslang neue Blutzellen gebildet. [3,4] Beim Fötus dagegen erfolgt die Blutbildung in Leber und Milz. Im NSB befinden sich besonders viele HSC, weil diese im letzten Schwangerschaftsdrittel über den Blutkreislauf ins Knochenmark „umziehen“ müssen. [5] Der Gehalt an HSC im NSB ist ca. 3-mal höher als im Knochenmark von erwachsenen Menschen. [4]
Wofür wird Nabelschnurblut medizinisch genutzt?
Der besondere Wert von Nabelschnurblut ist bereits seit Ende der 1980er-Jahre bekannt, 1989 wurde erstmals ein Kind mit Fanconi-Anämie damit behandelt. [6] Seitdem kam Nabelschnurblut über 60.000 Mal bei ca. 80 Indikationen zum Einsatz. [7,8]
Nabelschnurblut, mit den darin enthaltenen Stammzellen, kann sowohl allogen (= fremd, von anderen Personen) als auch autolog (= eigen) transplantiert werden, z. B. bei Krebserkrankungen, Blutbildungsstörungen und Immundefekten. [2,8]
Für die eigene Verwendung gewonnenes und gelagertes NSB ist schnell verfügbar und besonders verträglich. [7] Fast 1 Mio. NSB-Eigenspenden wurden in 24 europäischen Stammzellbanken privat eingelagert – bis Januar 2025 wurden davon 239 medizinisch genutzt: zur Regeneration von geschädigtem Gewebe oder um die Bildung von Blutzellen, z. B. nach einer Chemotherapie oder Bestrahlung, wiederherzustellen* (vgl. Abb. 2). [9]

Vita 34, FamiCord AG
Welches zukünftige Potenzial steckt im Nabelschnurblut?
NSB ist Gegenstand der medizinischen Forschung. Die Datenlage verbessert sich dabei stetig. Aktuelle Untersuchungen beschäftigen sich mit der Anwendung von NSB bei der Behandlung von:
- Erkrankungen des Blutes und des Knochenmarks [10-57]
- Solide Tumore [58-65]
- Autoimmunerkrankungen [66-69]
- Frühgeburtserkrankungen [70,71]
- Pädiatrische Krebserkrankungen [72,73]
- Seltene genetische Erkrankungen [74,75]
Was sind die Herausforderungen für die Anwendung von Nabelschnurblut?
Damit das NSB mit den enthaltenen Stammzellen im Bedarfsfall als Therapeutikum geeignet ist, muss eine ausreichende Menge an Zellmaterial gewonnen und eingelagert werden können. [3] Zentrale Herausforderungen sind dabei die begrenzte Menge des NSB, das bei der Geburt entnommen werden kann, sowie der Zeitpunkt des Abnabelns des Neugeborenen. [76,77] Außerdem sind entsprechende hochentwickelte Technologien zur Konservierung und Lagerung von NSB notwendig, um die Zellviabilität über Jahre und Jahrzehnte hinweg zu sichern. [78]
-> Lesen Sie mehr zum Thema Entnahme und Einlagerung von NSB
* Anwendungen im Rahmen der Zulassung/Genehmigung zur hämatologischen Rekonstitution und Immunrekonstitution nach Hochdosischemotherapie oder Bestrahlungstherapie oder im Rahmen von Heilversuchen oder klinischen Studien
Malhotra A et al. Pediatric Res. 2023;94:1631-1638
Galieva LR et al. Front Pharmacol. 2017;8:628
Smith BR. Yale J Biol Med. 1990;63(5):371-380
Bönig H et al. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz. 2011;54(7):791-796
Gao X et al. Development. 2018;145(2):dev139691
Gluckman E et al. N Engl J Med. 1989;321(17):1174-1178
Mayani H et al. Bone Marrow Transplant. 2020;55(1):48-61
Dessels C et al. Stem Cells Transl Med. 2018;7(9):643-650
Interne Daten der FamiCord AG. Januar 2025.
ClinicalTrials.gov. NCT01351545
ClinicalTrials.gov. NCT01451502
ClinicalTrials.gov. NCT04707300
ClinicalTrials.gov. NCT05110742
ClinicalTrials.gov. NCT05667155
ClinicalTrials.gov. NCT05669079
ClinicalTrials.gov. NCT06707259
ClinicalTrials.gov. NCT06712108
ClinicalTrials.gov. NCT06729320
ClinicalTrials.gov. NCT06792682
ClinicalTrials.gov. NCT06807606
ClinicalTrials.gov. NCT00012545
ClinicalTrials.gov. NCT01728545
ClinicalTrials.gov. NCT03016806
ClinicalTrials.gov. NCT03173937
ClinicalTrials.gov. NCT04628026
ClinicalTrials.gov. NCT05092451
ClinicalTrials.gov. NCT05584761
ClinicalTrials.gov. NCT05884333
ClinicalTrials.gov. NCT05929092
ClinicalTrials.gov. NCT06039436
ClinicalTrials.gov. NCT06109064
ClinicalTrials.gov. NCT06125483
ClinicalTrials.gov. NCT06351462
ClinicalTrials.gov. NCT06381817
ClinicalTrials.gov. NCT06534255
ClinicalTrials.gov. NCT06650553
ClinicalTrials.gov. NCT06680661
ClinicalTrials.gov. NCT01949129
ClinicalTrials.gov. NCT04347616
ClinicalTrials.gov. NCT04644016
ClinicalTrials.gov. NCT05014165
ClinicalTrials.gov. NCT05290662
ClinicalTrials.gov. NCT05842707
ClinicalTrials.gov. NCT06066359
ClinicalTrials.gov. NCT06105658
ClinicalTrials.gov. NCT06155188
ClinicalTrials.gov. NCT06464861
ClinicalTrials.gov. NCT06696846
ClinicalTrials.gov. NCT01656603
ClinicalTrials.gov. NCT03158896
ClinicalTrials.gov. NCT04990323
ClinicalTrials.gov. NCT05775718
ClinicalTrials.gov. NCT06480630
ClinicalTrials.gov. NCT06693791
ClinicalTrials.gov. NCT01962636
ClinicalTrials.gov. NCT06345495
ClinicalTrials.gov. NCT01962636
ClinicalTrials.gov. NCT03420963
ClinicalTrials.gov. NCT05703854
ClinicalTrials.gov. NCT06066424
ClinicalTrials.gov. NCT06358430
ClinicalTrials.gov. NCT04991870
ClinicalTrials.gov. NCT05922930
ClinicalTrials.gov. NCT06464965
ClinicalTrials.gov. NCT06083883
ClinicalTrials.gov. NCT06265220
ClinicalTrials.gov. NCT02932826
ClinicalTrials.gov. NCT03011021
ClinicalTrials.gov. NCT03835312
ClinicalTrials.gov. NCT05612919
ClinicalTrials.gov. NCT06427642
ClinicalTrials.gov. NCT05425043
ClinicalTrials.gov. NCT06631391
ClinicalTrials.gov. NCT02254863
ClinicalTrials.gov. NCT01861106
Frändberg S, et al. Cell Tissue Bank. 2016;17(3):439-448
Ciubotariu R, et al. Transfusion. 2018;58(6):1427-1433
Liedke S. et al. Stem Cells Tranlat. Med. 2024;13:30-42
Weitere Artikel

peopleimages.com - stock.adobe.com
Nabelschnurgewebe enthält besonders viele mesenchymale Stammzellen. Diese Vorläuferzellen können sich in spezialisierte Körperzellen, wie Knochen- oder Knorpelzellen, weiterentwickeln und deshalb für regenerative Therapien interessant sein. Ihr Potenzial kann durch eine vorsorgliche Einlagerung erhalten werden.

Vita 34, FamiCord AG
Nach einer Geburt ist die Versorgung des Neugeborenen und seiner Mutter das Wichtigste. Deshalb muss die Entnahme von Nabelschnurblut und -gewebe genau geplant sein und darf nur durch geschultes Kreißsaalpersonal in einer zertifizierten Geburtsklinik durchgeführt werden.
In Kooperation mit:
